Лабораторные опыты с водородом
Zn + H2SO4 = ZnSO4 + H2
Для ускорения реакции к серной кислоте добавляют немного сульфата меди.
Если нужно остановить реакцию, кислоту сливают с цинка во второе колено. Так получать водород проще, чем в аппарате Кирюшкина.
Чистый водород сгорает почти беззвучно, водород с воздухом -- со свистом. Выделяющийся водород можно поджечь, но пламя почти незаметно.
Водород вытесняет металлы из некоторых оксидов:
CuO + H2 = Cu + H2O
MoO3 + 3H2 = Mo + 3H2O
Метки: ВОДОРОД, Серная кислота, цинк, восстановление, оксид меди, оксид молибдена, медь, молибден
Равновесие образования роданидного комплекса железа (III)
3KSCN + FeCl3 = Fe(SCN)3 + 3KCl,
или, в ионной форме,
3SCN- + Fe3+ = Fe(SCN)3.
Реакция обратима. При разбавлении комплекс разрушается, что видно по ослаблению окраски. Если добавить железа или роданида, равновесие, по принципу Ле-Шателье смещается в сторону образования комплекса и окраска вновь усиливается.
Хлорид калия тоже разрушает комплекс, что часто интерпретируют как смещение равновесия влево по принципу Ле-Шателье. Однако реально KCl в этой реакции не участвует, так как взаимодействие происходит между ионами железа и роданид-ионами. Такая интерпретация также опровергается тем, что комплекс легко разрушается также сульфатом натрия (да и любыми другими солями).
Тому может быть два объяснения. Во-первых, фоновые электролиты способствуют диссоциации любых электролитов, экранируя их заряджы. Но тогда эффект хлорида калия и сульфата натрия был бы одинаковым. Во-вторых, образующийся при диссоциации комплекса ион Fe3+ гидролизуется с образованием Fe(OH)3, а фоновые электролиты способствуют его выпадению в осадок (причём тем сильнее, чем больше заряд иона).
Метки: роданид, Железо, равновесие, принцип Ле-Шателье
Гидролиз ацетата натрия
CH3COO- + H2O = CH3COOH + OH-
рН такого раствора чуть больше 8 и он слегка окрашивает фенолфталеин.
Если такой раствор нагреть, гидролиз усилится и окраска фенолфталеина станет более интенсивной.
В этом опыте мы сравниваем окраску фенолфталеина в одинаковых раствора ацетата натрия при охлаждении и нагревании. При нагревании окраска усиливается за счёт усиления гидролиза.
Метки: ацетат тнатрия, гидролиз, фенолфталеин
Поулчение жидкого аммиака (много) и растворение натрия в нём
Аммиак получают при нагревании по реакции
NaOH + NH4Cl = NaCl + NH3
От воды аммиак освобождают, пропуская через охлаждаемую водой со льдом ловушку, содержащую гидроксид натрия NaOH.
Осушенный таким образом аммиак улавливают в ловушке с сухим льдом в ацетоне (температура -70С).
Бинго! Получено около 3 мл жидкого аммиака.
Щелочные металлы растворяются в нём, давая глубоко синие растворы.
Метки: аммиак, натрий, сухоё лёд, гидроксид натрия
Получение хлора
Если залить твёрдый перманганат калия KMnO4 концентрированной соляной кислотой, то выделится хлор и образуется тёмно-зелёный раствор. То же самое наблюдается, если залить оксид марганца (IV) MnO2 концентрированной соляной кислотой. Это означает, что в продукте восстановления KMnO4 и MnO2 концентрированной соляной кислотой степень окисления марганца меньше, чем +4. Но она не может быть +2, поскольку растворы солей Mn(+2) почти бесцветные. Это зелёное вещество экстрагируется этилацетатом, то есть оно малополярно. Лучше всего этим наблюдениям соответсвует хлорид марганца (III) MnCl3 или соответсвующая комплекесная кислота HMnCl4:
2KMnO4 + 16HCl = 2MnCl3 + 4Cl2 + 2KCl + 8HCl
2MnO2 + 8HCl = 2MnCl3 + Cl2 + 4H2O
MnCl3 устойчив только при высокой концентрации хлоридов. При разбавлении он диспропорционирует:
2MnCl3 + 2H2O = MnO2 + MnCl2 + 2HCl
Поэтому в разбавленной (20%) кислоте MnCl3 не образуется: MnO2 вообще не реагирует с такой кислотой, а KMnO4 даёт коричневый осадок (скорее всего, MnO2):
И ничего общего с уравнением, которое пишут в учебниках, где марганец восстанавливается до MnCl2.
Если кислота разбавленная (хотя бы 20%), то MnCl3 в
хочется: Придушить авторов учебников, которые сдувают чушь друг у друга,
Метки: хлор, перманганат калия, оксид марганца, соляная кислота
Разложение хлората калия при нагревании
2KClO3 = 2KCl + 3O2
Без катализатора выделения газа не заметно. Идёт диспропорционирование:
4KClO3 = KCl + 3KClO4
Метки: хлорат калия, бертолетова соль, кислород, катализ, оксид хрома (III)
Реакция бромата калия с серной кислотой
2KBrO3 + 2H2SO4 = 2KHSO4 + Br2 + 3O2 + H2O
Это отличает бромат от хлората, который образует ClO2.
Метки: бромат калия, Серная кислота, Бром
Реакция железа с серой
Fe + S = FeS
Метки: Железо, сера, сульфид железа
Реакция железа с селеном
Fe + Se = FeSe.
Реакция экзотермична, процесс распространяется сам.
Метки: Железо, селен, селенид железа
Селеновая печень
3Se + 6NaOH = 2Na2Se + Na2SeO3 + 3H2O
Образующийся селенид натрия Na2Se с примесью полиселенидов -- розового цвета.
Метки: селен, гидроксид натрия, диспролпроционирвоание, селенид, селенат
Реакция фосфора с селеном
2P + 5Se = P2Se5.
Образующийся селенид легко гидролизуется водой с образованием крайне дурно пахнущего селеноводорода.
Метки: фосфор, селен, селенид фосфора
Разноцветные слои
3H2O2 + 2CrO3 + 3H2SO4 = 6H2O + 3O2 + Cr2(SO4)3,
частично -- превратился в синий пероксид хрома CrO5:
CrO3 + 2H2O2 = CrO5 + 2 H2O
CrO5 перешел в эфирный слой, окрасив его в синий цвет.
Перокид водорода не до конца перемешался, и на дне остался слой раствора CrO3
Метки: пероксид, хром, хромат, катализ, экстракция
Получение фосфина диспропорционированием гипофосфита
Если образовавшемся фосфином заполнить пробирку и поджечь, он со свистом сгорает.
Метки: фосфин, гипофосфит, диспропорционирование
Реакция метана с хлором
CH4 + Cl2 = CH3Cl + HCl
CH4 + 2Cl2 = CH2Cl2 + 2HCl
CH4 + 3Cl2 = CHCl3 + 3HCl
CH4 + 4Cl2 = CCl4 + 4HCl
Все продукты -- бесцветные жидкости либо газы.
Однако реально при соотношениях хлор:метан 2:1 и меньше образуется черная сажа:
СH4 + 2Cl2 = C + 4HCl
и только при больших соотношениях продукты похожи на хлорметаны.
Метки: метан, хлор, горение, сажа, стехиометрия
Горение смесей бутана с воздухом.
2C4H10+13O2 = 8CO2 + 10H2O.
Стехиометрического соотношение -- примерно 60 мл бутана на 2 л воздуха. Смесь горит, если соотношение отличается от стехиометрического не более, чем в 1.5 раза.
Бутан берут из зажигалки, для чего снимают с неё защитный кожух и надевают на трубку вывода газа тонкий шланг. Бутылку заполняют нужным объёмом воды из шприца и вытесняют воду бутаном. Состав смеси получается не очень точным, так как часть воды может вытесниться при удерживани бутылки. Кроме того, если поток бутана перекрыть не сразу после того, как он вытеснит воду, в бутылке может оказаться его некоторый избыток.
Метки: Бутан, воздух, горение, стехиометрия
Селенид натрия с сояной кислотой: что же там получается?
Метки: селенид натрия, соляная кислота, селеноводород, селен
Реакция натрия с селеном
2Na + Se = Na2Se
Чтобы продукты реакций не пришлось собирать с потолка, натрий кидают маленькими кусочками.
Метки: натрий, селен, горение, реакция соединения
Реакция кальция с селеном
Ca + Se = CaSe
Метки: кальций, селен, горение, реакция соединения
Реакция кальция с серой
Ca + S = CaS
Метки: кальций, сера, горение, реакция соединения
Получение нитрита натрия
NaNO3 + Pb = NaNO2 + PbO.
Действительно, в этой реакции свинец превращается в коричневое вещество, которое можно соотнести с оксидом PbO. Однако во что при этом превращается нитрат, неочевидно. Хотя бы потому, что после образования оксида свинца в системе идет выделение газа (это может быть кислород, выделяющийся при разложении избытка нитрата под каталитическим действием оксида свинца). А ещё потому, что если верить некоторым справочникам, температура разложения нитрита -- 218С (т.е. заведомо ниже, чем в нашей системе), а что при этом образуется -- непонятно.
Метки: нитрат, свинец, нитрит, оксид свинца
Попытка поджечь селен
Se + O2 = SeO2,
однако энергии, которая при этом выделяется, недостаточно для поддержания горения.
Получение и горение ацетилена
CaC2 + 2H2O = C2H2 + Ca(OH)2
Ацетилен энергично горит коптящим пламенем, его смеси с воздухом взрываются:
2C2H2 + 5O2 = 4CO2 + 2H2O
Если ацетилен в смеси с воздухом в избытке, то избыток за счет нагревания разлагается на простые вещества:
C2H2 = 2С + H2
Углерод С выделяется в виде сажи.
Если смесью ацетилена с воздухом заполнить пространство под жестяной банкой и поджечь, то банка може т подскочить.
Метки: карбид кальция, ацетилен, горение
Таблица Менделеева - ПРИЛОЖЕНИЕ в Мой Мир ))))) Пользуемся)))))
приложение ТАБЛИЦА МЕНДЕЛЕЕВА в Мой МИР:
Приложение Таблица Менделеева
http://my.mail.ru/apps/462883

Приложение Таблица Менделеева
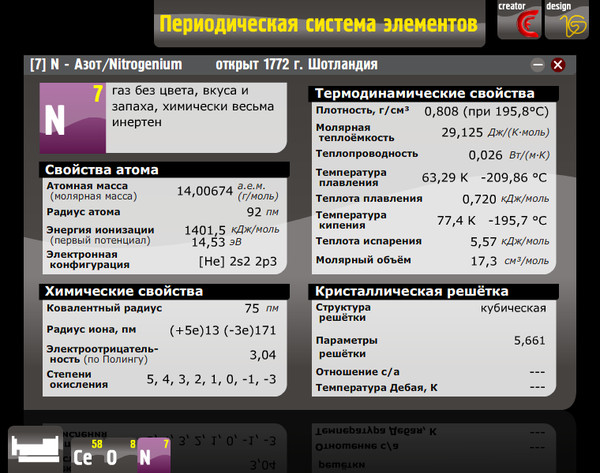
Приложение Таблица Менделеева
Метки: таблица Менделеева, химия, физика, периодическая система элементов
Чтобы их читать, Вам нужно вступить в группу
