Получение жидкого аммиака и растворение в нем натрия
2CaO + 2NH4Cl = CaCl2 + Ca(OH)2 + 2NH3
Перед ловушкой с охлаждающей смесью стоит еще одна ловушка с водой для предварительного охлаждения аммиака.
Жидкий аммиак -- бесцветная подвижная жидкость. Если в нее бросить натрий, он расвторится, при этом образуется темно-синий раствор. Он представляет собой сольватированные ионы Na+ и сольватированные же электроны. Именно за счет наличия сольватированных электронов расвтор и окрашен.
Метки: аммиак, сухой лед, натрий, сольватация
Реакция метана с хлором
CH4 + Cl2 = CH3Cl + HCl
CH4 + 2Cl2 = CH2Cl2 + 2HCl
CH4 + 3Cl2 = CHCl3 + 3HCl
CH4 + 4Cl2 = CCl4 + 4HCl
Все продукты -- бесцветные жидкости либо газы.
Однако реально при соотношениях хлор:метан 2:1 и меньше образуется черная сажа:
СH4 + 2Cl2 = C + 4HCl
и только при больших соотношениях продукты похожи на хлорметаны.
Метки: метан, хлор, горение, сажа, стехиометрия
Получение и свойства ацетилена
CaC2 + 2H2O = Ca(OH)2 + C2H2
Ацетилен, полученный из технического карбида кальция содержит разные примеси, придающие ему чесночный запах (видимо, фосфин PH3, арсин AsH3 и т.п.). Чтобы от них избавиться, газ пропускают через раствор I2 с KI в воде. I2 окисляет большую часть примесей и газ на выходе почти не пахнет.
Очищенный ацетилен, видимо, не реагирует с перманганатом калия (реакция, судя по тому, как медленно она идет, обусловлена примесями), зато дает превосходный коричневый осадок с аммиачным комплексом одновалентной меди (в этом ролике -- синего цвета, так как медь не удалось полностью восстановить):
[Cu(NH3)2]2SO4 + C2H2 = Cu2C2 + (NH4)2SO4 + 2NH3
С бромной водой чистый ацетилен тоже не реагирует.
Метки: ацетилен, перманганат калия, бромная вода, ацетиленид, этин
Сухой лёд в известковой воде
Ca(OH)2 + CO2 = CaCO3 + H2O
Далее осадок расвторяется в избытке CO2:
CaCO3 + CO2 + H2O = Ca(HCO3)2
Метки: сухой лёд, оксид углерода, известковая вода, реакция нейтрализации, кислая соль
Выделение водорода при реакции натрия с водой.
2Na + 2H2O = 2NaOH + H2
Если проводить эту реакцию без доступа кислорода к натрию, собрать выделяющийся водород и поджечь, то он загорится. Опыт нужно проводить аккуратно -- смесь водорода с воздухом может взорваться под стеклом и стекло разлетится.
Реакция метана с хлором
CH4 + 2Cl2 = C + 4HCl
Заполнение пластиковой бутылки хлором и метаном
Поджигание смеси лучиной
Поджигание смеси магнием
Индикаторная бумага в продуктах реакции
Горение свечи в кислороде
Горение магния под сухим льдом
2Mg + CO2 = 2MgO + C
Оставшийся уголь виден в виде черного порошка.
Метки: магний, сухой лёд, горение, углекислый газ
Попытка поджечь селен
Se + O2 = SeO2,
однако энергии, которая при этом выделяется, недостаточно для поддержания горения.
Сухой лёд в кипятке
Метки: сухой лёд, оксид углерода
Гидролиз тионилхлорида
SOCl2 + H2O = SO2 + 2HCl
К сожалению, тионилхлорид не смешивается с водой. Реакция идет на поверхности и поэтому -- довольно медленно. кроме того, она, видимо, обратима, поэтому, когда вода насыщается HCl, скорость выделения газа падает. Реакция поначалу экзотермична за счет растворения HCl в воде, а потом, после насыщения воды, становится эндотермичной.
Метки: тионилхлорид, Вода, гидролиз
Реакция оксида фосфора с водой
P2O5 + H2O = 2HPO3
При этом выделяется столько энергии, что вода закипает
Метки: Вода, оксид фосфора, гидратация
Получение оксида азота (III).
NO + NO2 = N2O3
Смесь NO и NO2 получают, действуя серной кислотой на нитрит калия KNO2:
2KNO2 + H2SO4 = K2SO4 + NO + NO2 + H2O
Перед ловушкой с охлаждающей смесью стоит ловушка с водой, которая предварительно охлаждает газовую смесь.
По книгам, N2O3 -- голубые кристаллы. У нас, правда, почему-то получилась жидкость. Возможно, дело во влаге, которая летела вместе с газами и образовала азотную кислоту.
Как насыпают нитрит калия в двухколенную пробирку.
Метки: оксид азота, нитрит, Серная кислота
Реакция тионилхлорида с водой
SOCl2 + H2O = SO2 + 2HCl
С водой он6 при этом не смешивается, поэтому реакции идет на границе раздела двух жидкостей (тионилхлорид тяжелее). К сожалению, реакция обратима, поэтому когда слой воды насыщается хлороводородом она почти останавливается. Но все равно, суммарный объем жидкостей заметно уменьшается. Что бы я не говорил на этой записи, реакция эндотермична, под конец пробирка заметно холодная.
Метки: тионилхлорид, гидролиз
Пары брома
Метки: Бром
Горение угля в кислороде.
C + O2 = O2
В кислороде он тлеет гораздо ярче.
Получение бромацетона -- автокаталитчиеская реакция
Метки: Бром, ацетон, автокатализ, бромацетон
Плавление селена.
Разложение хлората калия
4KClO3 = 3KCl + KClO4
При повышении температуры KClO4 начинает разлагаться:
KClO4 = KCl + 2O2
Если же нагревать хлорат калия в присутствии какого-нибудь катализатора, то он плавится и сразу разлагается:
2KClO3 = 2KCl + 3O2.
Если в качестве катализатора использовать Cr2O3, то он окрасится в оранжевый цвет. Это говорит о том, что хром из трехвалентного перешел в шестивалентный.
Метки: бертолетова соль, хлорат калия, кислород, оксид хрома, разложение диспропорционирование
Реакция бертолетовой соли с серной кислотой.
3KClO3 + H2SO4 = KClO4 + 2ClO2 + 2KHSO4 + H2O
Образущийся оксид хлора (IV) ClO2 -- ядовитый зеленый газ. Воспламеняет горючие вещества. Иногда разлагается самопроизвольно.
Метки: оксид хлора, Серная кислота, бертолетова соль, хлорат калия
Разложение хлората калия при нагревании
2KClO3 = 2KCl + 3O2
Без катализатора выделения газа не заметно. Идёт диспропорционирование:
4KClO3 = KCl + 3KClO4
Метки: хлорат калия, бертолетова соль, кислород, катализ, оксид хрома (III)
Определение кальция в полевых условиях
Общие замечания. Если щелочи добавлено мало, или индикатор разрушился, перехода окраски в фиолетовую наблюдаться не будет.
Химическая сущность. В сильнощелочной среде ионы магния выпадают в осадок в виде нераствори-мого Mg(OH)2, который не реагирует с ЭДТА. В результате ЭДТА оттитровавыаются только ионы кальция. Если в щелочи присутсвуют карбоаты, в осадок также выпадает CaCO3, что искажает результаты титрова-ния.
Метки: титрование, кальций, анализ воды, ЭДТА, комплексообразование, ПОЛЕВОЙ
Сжигание железной булавки в кислороде
2KMnO4 = K2MnO4 + MnO2 + O2
Чтобы зажечь в выделяющемся кислороде железную булавку, нужно наколоть на нее кусочек спички, поджечь ее, чтобы она тлела, и внести в пробирку, когда там идет выделение кислорода. Булавка будет гореть искрящимся пламенем.
3Fe + 2O2 = 2Fe3O4
Старайтесь не прикасаться горящей булавкой к стенкам пробирку -- прилипнет и погаснет.
Метки: Железо, кислород, перманганат калия, горение
Охлаждающая смесь (сухой лёд и ацетон)
Охлаждающую смесь лучше готовить не так, как на этом ролике (вы видите, что здесь половина ацетона выплеснулась из-за резкого выделения большого объема углекислого газа), а медленно приливая ацетон в стакан с сухим льдом.
Метки: сухой лёд, резина, охлаждающая смесь
Таблица Менделеева - ПРИЛОЖЕНИЕ в Мой Мир ))))) Пользуемся)))))
приложение ТАБЛИЦА МЕНДЕЛЕЕВА в Мой МИР:
Приложение Таблица Менделеева
http://my.mail.ru/apps/462883

Приложение Таблица Менделеева
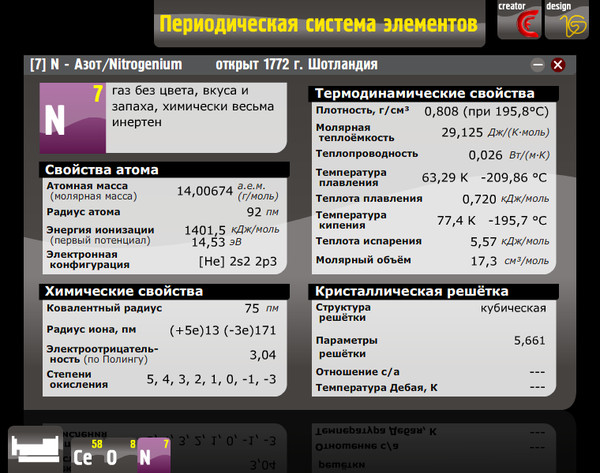
Приложение Таблица Менделеева
Метки: таблица Менделеева, химия, физика, периодическая система элементов
Чтобы их читать, Вам нужно вступить в группу
